La Química Orgánica es la rama de la química que estudia una clase numerosa de moléculas que contienen carbono formando enlaces covalentes carbono-carbono o carbono-hidrógeno, algunos grupos funcionales son : alcohol, éter , aldehído, cetona, entre otros.
En este presente trabajo les daremos a conocer sobre la química orgánica con respecto a un grupo funcional los Alcoholes, bueno estos son en un sentido general, tanto ácidos, como básicos. Este doble carácter queda patente por la tendencia de las moléculas de alcohol a asociarse a través de puentes de hidrógeno ,
Los alcoholes pueden ser primarios, secundarios, o terciarios, en función del número de átomos de hidrógeno sustituidos en el átomo de carbono al que se encuentran enlazado el grupo hidroxilo y a su vez podemos encontrar sobre su clasificación según el número de grupos hidroxilos.
sábado, 25 de junio de 2011
viernes, 24 de junio de 2011
Alcoholes
Los alcoholes son compuestos orgánicos que contienen un grupo hidróxilo (-OH), que se encuentra unido a una cadena hidrocarbonada a través de un enlace covalente a un átomo de carbono con hibridación sp3, mientras que los compuestos que poseen un grupo hidróxilo unido a uno de los átomos de carbono de un doble enlace se conocen como enoles, y los compuestos que contienen un grupo hidróxilo unido a un anillo de benceno se llaman fenoles
clasificación de los alcoholes
Los alcoholes se clasifican en primarios, secundarios y terciarios, dependiendo del carbono funcional al que se una el grupo hidroxilo.
- Alcohol primario: se utiliza la Piridina (Py) para detener la reacción en el aldehído Cr03 / H+ se denomina reactivo de Jones, y se obtiene un ácido carboxílico.
- Alcohol secundario: se obtiene una cetona + agua.
- Alcohol terciario: si bien se resisten a ser oxidados con oxidantes suaves, si se utiliza uno enérgico como lo es el permanganato de potasio, los alcoholes terciarios se oxidan dando como productos una cetona con un número menos de átomos de carbono, y se libera metano.
Y a su vez los alcoholes se pueden clasificar según el número de grupos hidroxilos que contenga el compuesto:
- Monoalcohol o Monol: Son alcoholes que tienen un solo grupo hidroxilo (–OH), y son aquellos que pueden clasificarse como alcoholes primarios, secundarios y terciarios.
- Polialcoholes: Son compuestos que tienen dos o más grupos hidroxilos (–OH).
Nomenclatura de alcoholes

2. Se numera la cadena principal para que el grupo -OH tome el localizador más bajo. El grupo hidroxilo tiene preferencia sobre cadenas carbonadas, halógenos, dobles y triples enlaces.
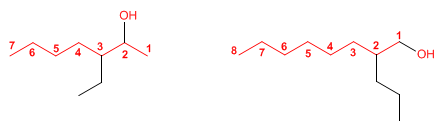
3. El nombre del alcohol se construye cambiando la terminación -o del alcano con igual número de carbonos por -ol
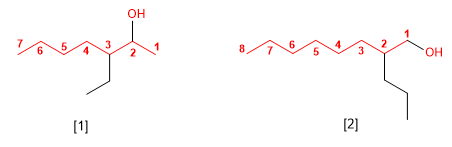
4. Cuando en la molécula hay grupos grupos funcionales de mayor prioridad, el alcohol pasa a serun mero sustituyente y se llama hidroxi-. Son prioritarios frente a los alcoholes: ácidos carboxílicos, anhídridos, ésteres, haluros de alcanoilo, amidas, nitrilos, aldehídos y cetonas.
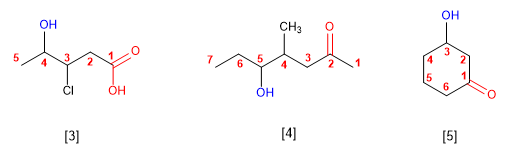
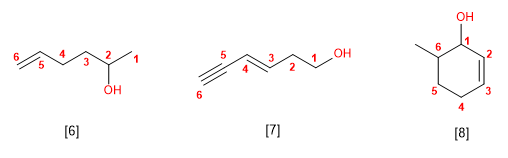
5. El grupo -OH es prioritario frente a los alquenos y alquinos. La numeración otorga el localizador más bajo al -OH y el nombre de la molécula termina en -ol.
Usos
Los alcoholes se utilizan como productos químicos intermedios y disolventes en las industrias de textiles, colorantes, productos químicos, detergentes, perfumes, alimentos, bebidas, cosméticos, pinturas y barnices. Algunos compuestos se utilizan también en la desnaturalización del alcohol, en productos de limpieza, aceites y tintas de secado rápido, anticongelantes, agentes espumígenos y en la flotación de minerales.
PROPIEDADES FÍSICAS DE LOS ALCOHOLES
se basan principalmente en su estructura. El alcohol esta compuesto por un alcano y agua. Contiene un grupo hidrofóbico (sin afinidad por el agua) del tipo de un alcano, y un grupo hidroxilo que es hidrófilo (con afinidad por el agua), similar al agua. De estas dos unidades estructurales, el grupo –OH da a los alcoholes sus propiedades físicas características, y el alquilo es el que las modifica, dependiendo de su tamaño y forma.
Reacción como bases El grupo hidroxilo de los alcoholes puede ser reemplazado por diversos aniones ácidos reaccionando, por lo tanto, como una base según la ecuación general siguiente, en la que se obtiene un haluro de alquilo como producto: H2 R - OH + H - X → R - X + O
Solubilidad :
Puentes de hidrógeno: La formación de puentes de hidrógeno permite la asociación entre las moléculas de alcohol. Los puentes de hidrógeno se forman cuando los oxígenos unidos al hidrógeno en los alcoholes forman uniones entre sus moléculas y las del agua. Esto explica la solubilidad del metanol, etanol, 1-propanol, 2-propanol y 2 metil-2-propanol.
|
| ||
| A partir de 4 carbonos en la cadena de un alcohol, su solubilidad disminuye rápidamente en agua, porque el grupo hidroxilo (–OH), polar, constituye una parte relativamente pequeña en comparación con la porción hidrocarburo. A partir del hexanol son solubles solamente en solventes orgánicos. | |||
|
| ||
Los puntos de ebullición de los alcoholes también son influenciados por la polaridad del compuesto y la cantidad de puentes de hidrógeno. Los grupos OH presentes en un alcohol hacen que su punto de ebullición sea más alto que el de los hidrocarburos de su mismo peso molecular. En los alcoholes el punto de ebullición aumenta con la cantidad de átomos de carbono y disminuye con el aumento de las ramificaciones
Deshidratación de alcoholes
La deshidratación de alcoholes es el proceso químico que consiste en la conversión de un alcohol en un alqueno por proceso de eliminación. Para realizar este procedimiento se utiliza un ácido mineral para extraer el grupo hidroxilo (OH) desde el alcohol, generando una carga positiva en el carbono del cual fue extraído el OH el cual tiene una interacción eléctrica con los electrones más cercanos (por defecto, electrones de un hidrógeno en el caso de no tener otro sustituyente) que forman un doble enlace en remplazo.
Por esto, la deshidratación de alcoholes útil, puesto que fácilmente convierte a un alcohol en un alqueno.
Un ejemplo simple es la síntesis del ciclohexeno por deshidratación del ciclohexanol. Se puede ver la acción del ácido (H2SO4) ácido sulfúrico el cual quita el grupo hidroxilo del alcohol, generando el doble enlace y agua.
Anexo : estos son algunos de los alcoholes más usados a nivel mundial.
| Alcohol | Forma estructural |
|---|---|
| Metanol |  |
| Etanol |  |
| Propanol | 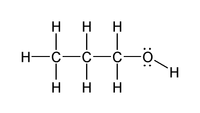 |
| Butanol |
Conclusión :
A través de este presente trabajo se dio a conocer sobre la química orgánica y detalladamente sobre su grupo funcional alcoholes, sobre sus tipos de usos que se le dan, como se clasifican, sobre las propiedades físicas y químicas, sobre su nomenclatura, su solubilidad, entre otros.
Finalmente se puede deducir que el alcohol es un importante grupo funcional ya que se encuentra extensamente en la vida natural.
Suscribirse a:
Entradas (Atom)